Las mutaciones son cambios en la secuencia de nucleótidos en el genoma viral que pueden generar alteraciones en la secuencia de aminoácidos de las proteínas que codifica.
Al igual que cualquier otro organismo, los virus cambian con el tiempo. Debido a que son entes genómicos y a su elevada tasa de replicación, la velocidad a la que estos cambios (mutaciones) aparecen y son transmitidos a las siguientes generaciones es tremendamente elevada. Cuando una o varias de estas mutaciones se mantienen en el tiempo consideramos que existe una “variante” nueva. Cuando se cumplen dos años de la aparición del más reciente de los coronavirus humanos, el SARS-CoV-2, repasamos qué variantes han aparecido y cómo pueden condicionar la evolución de la pandemia.
Las mutaciones son cambios en la secuencia de nucleótidos en el genoma viral que pueden generar alteraciones en la secuencia de aminoácidos de las proteínas que codifica. Estas se producen al azar: de hecho, la mayoría tienen poco o ningún impacto en el virus. Sin embargo, algunas pueden afectar a propiedades fundamentales como la afinidad por el receptor viral en la superficie de la célula hospedadora o la velocidad de la replicación de su genoma.
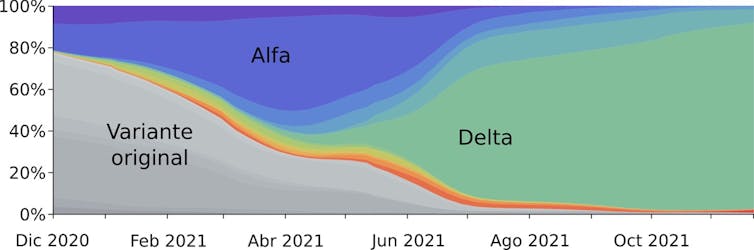
Si las mutaciones son deletéreas (nocivas) para el virus, serán rápidamente eliminadas de la población. Si son beneficiosas, bien por que aumentan la infectividad y/o la capacidad para replicarse, bien por que permiten al virus escapar de las defensas del organismo hospedador, esa variante del virus tendrá una ventaja frente al resto (Figura 1).
La nomenclatura de las variantes puede ser compleja. La OMS ha asignado etiquetas fáciles de recordar para las variantes clave: letras del alfabeto griego como alfa, beta, gamma y delta. Estas no reemplazan los nombres científicos existentes, ya que estos contienen información científica importante.
Tipos de variantes
Según su interés desde un punto de vista sanitario la OMS agrupa a las múltiples variantes en:
Variantes bajo escrutinio (Variants Under Monitoring, VUM): con cambios genéticos que se sospecha podrían afectar a las características del virus. En este caso se recomienda la evaluación de las propiedades del virus.
Variantes de interés (Variants Of Interest VOI): con cambios genéticos que podrían o se sabe que están relacionados con la transmisión del virus, la gravedad y el tratamiento de la enfermedad, la capacidad del virus para evadir el sistema inmune o el diagnóstico de la infección. Estas se asocian con una transmisión comunitaria significativa, es decir, presencia relativa creciente o un número creciente de casos, entre otros factores epidemiológicos.
Variantes de preocupación (Variants Of Concern VOC): cumplen con los requisitos de las anteriores y, a través de una evaluación comparativa, se ha demostrado que están asociadas con uno o más de los siguientes cambios: aumento de la transmisibilidad, aumento de la virulencia o cambio en la presentación clínica de la enfermedad, reducción de la eficacia de las medidas sociales y de salud pública o de los diagnósticos, vacunas y terapias disponibles.
La aparición de la variante ómicron
La variante ómicron se notificó por primera vez a la OMS desde Sudáfrica el 24 de noviembre de 2021. La situación epidemiológica en el país africano se ha caracterizado por tres picos distintos en los casos notificados y la variante delta fue predominante en el último pico (como en el resto del mundo, ver Figura 1).
En los últimos días, las infecciones han aumentado de forma pronunciada, coincidiendo con la detección de ómicron. Esta variante tiene una gran cantidad de mutaciones, muchas de ellas en el gen que codifica para la proteína de la espícula o proteína S (Figura 2). Alguna de estas mutaciones son preocupantes ya que podrían estar implicadas en la unión de la proteína S al receptor ACE2 y en la evasión del sistema inmune.
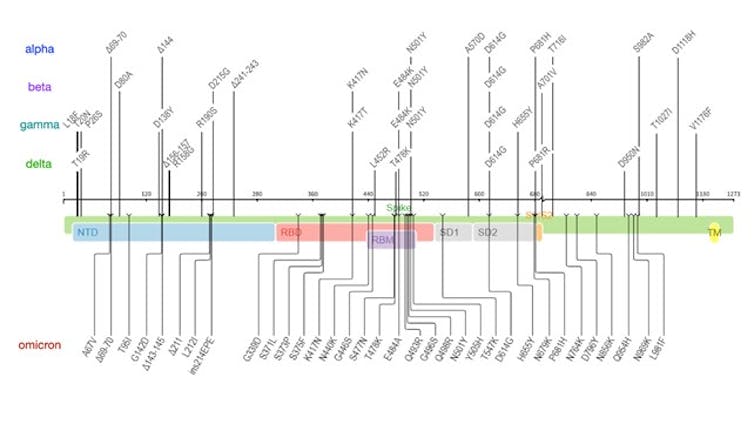
¿Cómo reaccionan las vacunas a las variantes?
En estos dos años en los que han surgido las cinco variantes de preocupación mencionadas se ha conseguido el hito histórico de desarrollar un conjunto de vacunas que han demostrado una eficiencia extraordinaria.
Una de las preguntas principales en relación con la variante ómicron es si las vacunas funcionarán. Tras la vacunación, el sistema inmunológico genera una variedad de anticuerpos contra el antígeno (en este caso la proteína S). Es decir, se producen anticuerpos que reconocen varias partes de la proteína del virus frente a la cual nos han vacunado. Si algunas de estas partes cambian, es posible que los anticuerpos que se unían a esa región ya no la reconozcan tan eficientemente y, por lo tanto, dejen de funcionar.
Cuantos más cambios en la proteína, mayor probabilidad de que el virus evite la unión de los anticuerpos generados por la vacuna. Sin embargo, un virus no puede cambiar indefinidamente, existen regiones que han de mantenerse constantes para que la proteína pueda adoptar su estructura trimérica y ejercer su función de manera efectiva.
Por lo tanto, es posible que la vacunación haya fomentado la generación de anticuerpos frente a estas regiones comunes, con lo que incluso en presencia de las mutaciones tengamos cierto grado de protección. Además de la respuesta basada en anticuerpos, la vacunación también genera una respuesta mediada por linfocitos T. La activación de estas células no depende de reconocimiento de la proteína S en su forma plegada, sino de fragmentos de la misma que son presentados por la célula infectada. De nuevo, entre los fragmentos reconocidos hay muchos que corresponden a regiones conservadas, y por tanto las vacunas seguirán cumpliendo su función.
En resumen, podemos esperar una disminución en la eficiencia de la vacuna frente a esta variante en comparación con la cepa original, al igual que ocurrió con variantes anteriores. ¿Cuánta protección hemos perdido? Pronto lo sabremos.
Siguientes pasos contra ómicron
Para evitar una pérdida completa de la eficacia de la vacuna deberíamos entrenar el sistema inmune frente a diferentes variantes. Es decir, vacunar frente a múltiples variantes, lo cual es relativamente sencillo (técnicamente) con las plataformas de vacunas actuales.
Podríamos actualizar la vacuna (incluyendo la última de las variantes) o incluso crear un cóctel de múltiples variantes. Esta última estrategia tiene un beneficio extra. El sistema inmune es capaz de reconocer partes comunes en diversos antígenos, es decir, la producción de anticuerpos se centra en las regiones que se repiten. Como hemos comentado antes, es posible que algunas de estas regiones conservadas sean importantes o incluso fundamentales para el virus por lo que no se prevé que vayan a variar.
Además, es razonable pensar que futuras variantes mantendrían constante dichas regiones. Así pues, una aproximación vacunal como las mencionadas anteriormente nos proporcionaría, potencialmente, una mejor inmunidad frente a futuras nuevas variantes. Deberíamos utilizar la tercera dosis o dosis de refuerzo como una oportunidad para presentar a nuestro sistema inmune nuevas variantes. La tecnología necesaria para ello está puesta a punto.![]()
Luis Martinez-Gil, Profesor del Dep. de Bioquímica, Universitat de València y Ismael Mingarro, Catedrático de Bioquímica y Biología Molecular, Universitat de València
Este artículo fue publicado originalmente en The Conversation. Lea el original.








![¡En plena audiencia! Acusado atacó a jueza que le negó la libertad condicional [VIDEO]](https://e.rpp-noticias.io/small/2024/01/04/mmd-vd-20240104-clj-usa-justiciacriminalidad-349g2vy-es-1520871mp4_1520872.webp)







![BTS emociona al ARMY con tráiler de lo que será su primer concierto transmitido en Netflix [VIDEO] BTS emociona al ARMY con tráiler de lo que será su primer concierto transmitido en Netflix [VIDEO]](https://f.rpp-noticias.io/2026/03/04/385638_1844910.jpg?width=320&quality=80)
